|
||||

Определение корреляции показателя CT и титра вируса африканской чумы свиней в биологических жидкостяхУДК 619:616.98-076[:578.833.31 Мазлум Али, Власова Н.Н., Аронова Е.В., Иголкин А.С. ФГБУ"ВНИИЗЖ", г. Владимир Введение. Метод, позволяющий определять количество инфекционных единиц вируса в различных образцах, является необходимым инструментом в вирусологии. В исследовательских лабораториях титр вируса, вызывающего цитопатический эффект в культуре клеток, обычно рассчитывают, исходя из количества пораженных единиц культуры клеток (лунки, флаконы), после внесения в них серийных разведений исходного вируссодержащего материала и выражают в тканевых цитопатических дозах - ТЦД50, если эффект наблюдается у половины инфицированных проб [13].
Использование данного метода требует продолжительного периода времени: от 3 до 10 дней в зависимости от свойств исходного вируса. С появлением новых технологий для определения титра вируса в пробе все чаще применяют метод ПЦР в реальном времени (ПЦР-РВ). По данным Van Guilder HD, Vrana KE, Freeman WM (2008) ПЦР-РВ (или количественная ПЦР) лабораторный метод, основанный на циклической амплификации определенных фрагментов генома, который используется для одновременной индикации возбудителя и измерения количества молекул ДНК. В свою очередь, после проведения соответствующих расчетов его результаты позволяют определить титр вируса в испытуемой пробе [22].
Возбудителем африканской чумы свиней (далее, АЧС) является ДНК-содержащий вирус семейства Asfarviridae, рода Asfivirus [2, 3, 8, 12]. Поскольку геном вируса АЧС представлен ДНК, в отличие от детекции геномов РНК-содержащих вирусов, для его обнаружения методом ПЦР-РВ не требуются получения кДНК, что, как минимум, на 1 час сокращает время исследований и составляет с этапом выделения ДНК 2 часа 30 минут.
Для титрования вируса АЧС используют первичные культуры клеток (культура клеток костного мозга свиней, культура лейкоцитов свиней, альвеолярных макрофагов свиней, почек свиней и селезенки свиньи), обладающие высокой чувствительностью [3, 4].
При культивировании в первичных культурах клеток свиньи вирус АЧС вызывает специфическую гемадсорбцию и оказывает цитопатогенное воздействие. Постановка реакции гемадсорбции (РГАд) является наиболее специфичным и чувствительным методом идентификации вируса АЧС, поскольку ни один из вирусов, поражающих свиней, не вызывает проявления гемадсорбции. Согласно рекомендации МЭБ, РГАд используется в качестве референтной методики выявления вируса АЧС, несмотря на трудоемкость постановки и продолжительность реакции (5-7 дней) [3, 4, 16, 20].
Исходя из вышеизложенного, при выполнении ряда лабораторных исследований и определении количества вируса в пробе в определенных случаях целесообразно заменить традиционные методы и использовать такие технологии, как ПЦР-РВ для проведения быстрого и эффективного анализа уровня накопления вируса.
Порогового значение цикла (Ct), фиксируемое в результате ПЦР-РВ, дает точные и воспроизводимые результаты с низкими стандартными отклонениями [21, 22].
Кроме того, ПЦР-РВ позволяет проводить абсолютную количественную оценку содержания нуклеиновых кислот в пробе при наличии референтной матрицы ДНК с известной концентрацией и количеством копий [24].
К другим преимуществам ПЦР-РВ относится быстрая и эффективная возможность сравнения и качественной оценки исследуемых образцов.
Так, в зарубежной литературе представлен ряд работ, в которых 4 демонстрируется определение вирулентности вируса по его содержанию в крови, отмечая, что скорость изменения С (соответственно, скорость увеличения титра в крови) у аттенуированного вируса ниже, чем у вирулентного [14, 18]. В своей работе Lacasta Anna et al. показали, что у животных, инфицированных аттенуированным штаммом вируса АЧС, наблюдалась более поздняя регистрация вирусной ДНК. Они выявляли вирус в назальных экскретах и крови только на 7-й день после инфицирования, причем, титр накопления вируса был в среднем ниже на 4-5 lg, чем у свиней, инфицированных вирулентным штаммом E75, и не превышал значений 104-5 ГАдЕ50/мл [18].
В другой работе Lewis T. et. al. показали, что делеция гена 9GL у вируса АЧС изолята Malawi Lil-20/1 (MAL) влияет на созревание ви-риона и репродукцию вируса в макрофагах и ослабляет вирусную инфекцию у свиней. Животные, инфицированные этим аттенуированным изолятом, оставались клинически здоровыми и демонстрировали увеличение значения Ot, выявляемое в ПЦР-РВ, что соответствовало снижению титра вируса в крови в 100-10 000 раз по сравнению с неделетированным изолятом Malawi Lil-20/1 [14].
Использование ПЦР-РВ в диагностике АЧС имеет еще одно преимущество перед РГАд, так как при постановке последнего невозможно выявление негемадсорбирующих вариантов вируса, как правило, у свиней с хронической или бессимптомной формой течения болезни. Следует также учитывать, что специфическая ГАд, хотя и является характерным признаком вирулентных вариантов вируса АЧС, отдельные негемадсорбирующие изоляты также могут быть высоковирулентными [15].
Таким образом, целью наших исследований являлось определение корреляции показателя Ct в ПЦР в режиме реальном времени и значений титра вируса, устанавливаемого в реакции гемадсорбции, а также расчета количества копий генома вируса АЧС в пробе.
Материалы и методы исследований. В представляемых экспериментах для титрования и накопления вируса АЧС использовали культуры клеток селезенки свиньи (СС) и костного мозга свиней (КМС), приготовленных в соответствии с методическими рекомендациями, разработанными в референтной лаборатории по АЧС ФГБУ «ВНИИЗЖ» [9, 10].
Расчет титра вируса проводили по методу Рида и Менча, или по методу Кербера в модификации Ашмарина через 7 дней после начала эксперимента [9, 10].
В качестве источника геномной ДНК и для заражения культуры клеток или титрования исходного вируса в работе использовали вирус АЧС изолят Krasnodar 07/17, выделенный в июле 2017 года из пробы селезенки павшей домашней свиньи (Краснодарский край). Накопление вируса осуществляли путем его пассирования в первичной культуре клеток СС в течение 2-3 пассажей.
Выделение вирусной ДНК из вируссодержащих образцов проводили с помощью набора «ДНК-сорб-Б» (ООО «НекстБио», Россия) в соответствии с инструкцией производителя [5].
Для детекции генома вируса АЧС использовали тест-систему «АЧС» для выявления вируса африканской чумы свиней методом полимеразной цепной реакции (ФБУН «ЦНИИ») [6], а также методику по выявлению генома вируса африканской чумы свиней методом полимеразной цепной реакции в режиме реального времени (ФГБУ «ВНИИЗЖ») [11].
Для получения и накопления ПЦР-продукта использовали: матричную ДНК вируса АЧС изолят Krasnodar 07/17 в объеме 5 мкл на реакцию, Taq-ДНК-полимеразу - 0,5 мкл, 10*буфер с (NH4)2SO4 - 2 мкл, смесь дезоксинуклеотидтрифосфатов 10 мМ - 0,5 мкл (Fermentas), праймеры, фланкирующие ген B646L (табл. 1) (по 10 пМ каждого), и 2 мкл 25мМ MgCl2. Объем деионизированной воды рассчитывали, исходя из общего объема реакционной смеси, равного 20 мкл. Режим амплификации использован согласно работе Neilan J.G. и др., 2004 [19]. Таблица 1. Праймеры, использованные для амплификации гена B646L вируса АЧС
Результаты амплификации гена B646L оценивали с помощью электрофореза в 1,0% агарозном геле.
Для элюции ПЦР-продукта из геля агарозы использовали «набор реагентов для элюции ДНК из агарозных гелей» (Qiagen) в соответствии с инструкцией производителя [7].
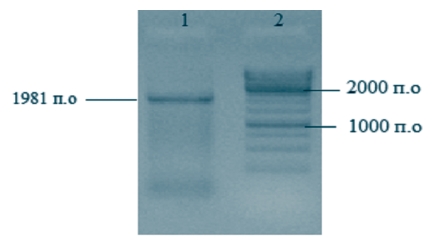
Результаты и их обсуждение. Поскольку в диагностике АЧС ПЦР-РВ используется как количественный метод (когда в реакции с использованием известной концентрации ДНК и количества копий гена по значению Ct определяется соотношение значения Ct к количеству копий), первым этапом работы являлось определение с помощью набора ФБУН «ЦНИИ» минимального количества копий генома вируса АЧС в образцах. Для этого с помощью ПЦР был амплифицирован полноразмерный ген B646L вируса АЧС. После проведения электрофореза на 1,0% агарозном геле (рисунок 1) продукт был элюирован из геля и его концентрация определена на спектрофотометре.
Рис. 1. Результаты электрофоретического разделения в 1% геле агарозы ПЦР-продукта (вирус АЧС изолят Krasnodar 07/17): трек 1 - электрофорез ПЦР-продукта полноразмерного гена B646L; трек 2 - маркер 1к (производитель ThermoFisher) с линейкой фрагментов от 10000 п.о. до 250 п.о. Количество копий гена B646L в данном образце рассчитано по формуле для «абсолютной оценки количества копий»: количество копий гена = (концентрация ПЦР продукта (нг) х 6,022*10-23)/ (длина ПЦР продукта (п.о.)х109 х 650)
Поскольку размер амплифицированного фрагмента 1981 п.о. и его концентрация после очистки из агарозного геля составляла 25,1 нг/мкл, рассчитанное количество копий гена составляло 1,17x1с11 копий/мкл.
На втором этапе исследований приготовили 10 десятикратных разведений образца ПЦР-продукта и провели их анализ в ПЦР-РВ с трехкратной повторностью. Результаты представлены в таблице 2.
Таблица 2. Значение Ct в ПЦР-РВ при разных концентрациях амплификата гена B646L вируса АЧС (n=3)
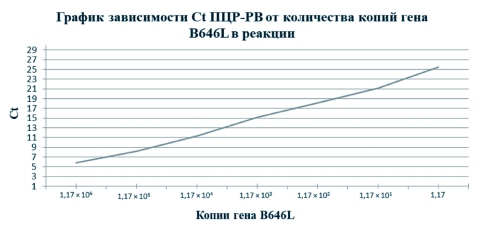
Полученные результаты ПЦР-РВ продемонстрировали обратно пропорциональную линейную зависимость показателя Ct от количества копий гена B646L вируса АЧС, когда снижение концентрации в 10 раз приводит к увеличению Ct на 3 цикла (рисунок 2).
Рис. 2. Корреляция значений Ct ПЦР-РВ с количеством копий гена B646L Таким образом, в результате экспериментов было установлено, что при высокой концентрации ДНК в образцах (>1,17x10 копий генома) реакция ПЦР-РВ может приводить к ложно отрицательному результату, поскольку чрезмерное количество исходной матрицы препятствует отжигу праймеров на амплифицированных матрицах, а когда количество копий снижается ПЦР-РВ позволяет обнаруживать геном вируса АЧС вплоть до минимального количества копий - 11,7 копии/мкл. Так как для постановки реакции используется 10 мкл матричной ДНК, чувствительность ПЦР-РВ в данных опытах составляет 117 копий.
На следующем этапе для наиболее точного определения титра вируса АЧС в пробе с помощью реакции гемадсорбции, провели сравнительный анализ чувствительности первичных культур клеток.
С этой целью параллельно заразили культуры клеток СС и КМС вирусом АЧС изолят Krasnodar 07/17 в дозе 103 ГАдЕ50 на матрас (объем 50 мл), и наблюдали за репродукцией вируса в культуре клеток. Из каждого матраса на седьмые сутки отобрали по 300 мкл культуральной жидкости, исследовали данные образцы методом ПЦР-РВ и определяли титр вируса АЧС в обеих культурах клеток в РГАд. Р результате титр вируса АЧС в культуре клеток СС составил 106 ГАдЕ50, а титр вируса АЧС в культуре клеток КМС составил 105 ГАдЕ50, то есть на 1lg ниже. Полученные данные также были подтверждены методом ПЦР-РВ, где значение Ct на седьмой день в культуре клеток СС составило 12,2, а в культуре клеток КМС 15,9.
Поскольку обе культуры клеток были использованы для заражения одной и той же дозой вируса, а репродукция вируса АЧС в культуре клеток СС показала более высокую чувствительность данной культуры к вирусу, для выполнения дальнейших этапов работы была выбрана культура клеток СС, как наиболее соответствующая целям исследований.
На следующем этапе работы устанавливали наличие корреляции значений Ct ПЦР-РВ с титром вируса в культуре клеток СС в РГАд. Для этого определили титр вируса АЧС изолята Krasnodar 07/17 в культуре клеток СС в соответствии с методическими рекомендациями, разработанными в референтной лаборатории по АЧС ФГБУ «ВНИИЗЖ» [9, 10].
В ходе исследований титр исходного вируса составил 7,0 ГАдЕ/ см3, материал которого использовали для приготовления семи десятикратных разведений. Для достоверности анализа все десятикратные разведения проб использовали для выделения ДНК вируса АЧС и постановки ПЦР-РВ с набором ФБУН «ЦНИИ» в трех повторностях. Для объективной оценки результатов реакции вычисляли среднее значение Ct, стандартное отклонение и пределы 95%-го доверительного интервала (табл. 3).
Таблица 3. Значение Ct ПЦР в реальном времени при разных разведениях вируса АЧС (n = 3)
Примечание: Н.З - нет значения Ct; * - внутренний контроль выделения ДНК; ** - среднее значение рассчитано по формуле:
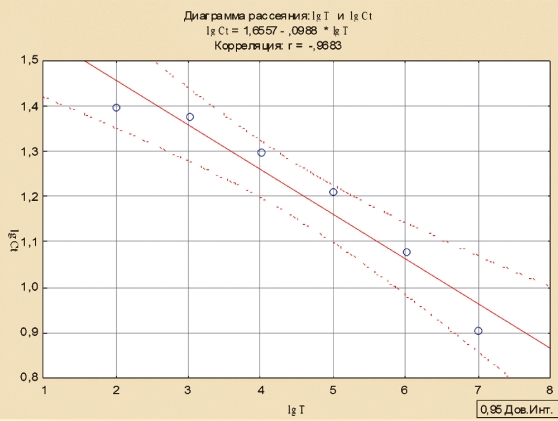
Для определения формулы расчета титра вируса построили линию регрессии и рассчитали коэффициент корреляции между логарифмом титра вируса и логарифмом Ct с помощью программы Statistica (рисунок 3)
Рис. 3. График зависимости между логарифмом титра вируса АЧС и логарифмом значения Ct ПЦР-РВ В наших исследованиях, коэффициент корреляции составил 0,9683, что свидетельствует о высокой достоверности (точности) исследований и позволяет производить вычисление титра вируса в пробе.
Таким образом, при анализе корреляции между показателями Ct ПЦР-РВ и результатами титрования проб в культуре клеток СС удалось установить близкую к линейной зависимость показателя Ct от титра вируса АЧС. Необходимо отметить, что в данном случае снижение концентрации на 1,0 lg, приводило к увеличению Ct на 4 цикла (рисунок 4).
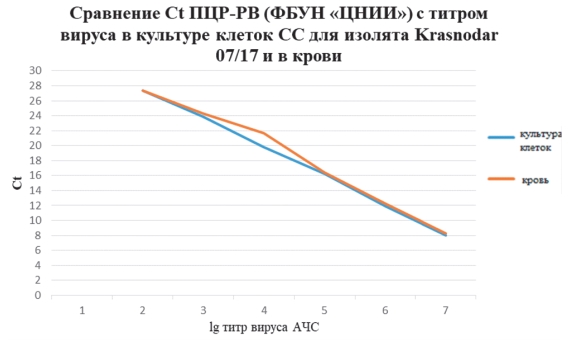
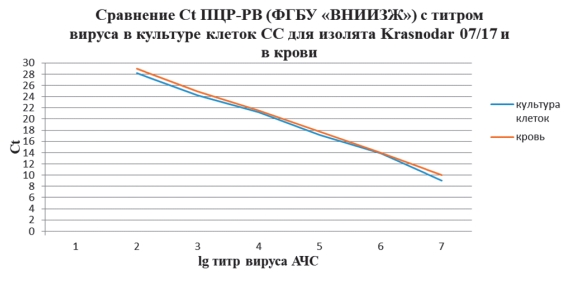
Следующим этапом нашей работы являлось определение аналогичного соответствия показателей Ct ПЦР-РВ с титром вируса, полученного из крови инфицированного животного вирусом АЧС изолят Krasnodar 07/17, павшего на 7 сутки после заражения (титр вируса в крови составлял 7,0 lg ГАдЕ/см3). Аналогично опытам с изолятом Krasnodar 07/17 в культуре клеток СС, образцы крови также использовали для приготовления 7 десятикратных разведений для исследования методом ПЦР-РВ в 3 повторностях. Сравнение результатов экспериментов и определение соотношения значений Ct и титра вируса продемонстрировало практически полную идентичность полученных результатов (рисунок 4).
Рис. 4. Значение Ct ПЦР-РВ в соотношении с титром вируса АЧС в культуре клеток и в крови инфицированной свиньи Результаты Ct обоих экспериментов в культуре клеток и в крови показали высокий уровень достоверности.
По результатам, представленным на рисунке 4, видно равномерное снижение значения Ct на 4 цикла при каждом последующем десятикратном разведении (то есть при увеличении титра на один логарифм). Следовательно, корреляция выражается в линейной зависимости соотношения Ct и титра вируса, подъем значения Ct каждые 4 цикла соответствовал снижению титра вируса на 1 lg.
Аналогичным образом проводили определение корреляции титра вируса и значений Ct для методики по выявлению генома вируса африканской чумы свиней методом полимеразной цепной реакции в режиме реального времени, разработанного в ФГБУ «ВНИИЗЖ» [11], которое дало аналогичные результаты (рисунок 5). Таким образом, полученные графики могут быть использованы для определения титра вируса АЧС в образцах крови и культуре клеток при исследовании методом ПЦР-РВ.
Рис. 5. Значение Ct ПЦР-РВ в соотношении с титром вируса АЧС в культуре клеток и в крови инфицированной свиньи На основании проведенных исследований можно сделать вывод о том, что для предварительной оценки титра вируса АЧС в инфицированной культуре клеток или крови зараженного животного целесообразно использовать, как тест-систему «АЧС» для выявления вируса африканской чумы свиней методом полимеразной цепной реакции (производитель ФБУН «ЦНИИ»), так и разработанную в ФГБУ «ВНИИЗЖ». Различие в показателях Ct для проб, исследуемых по методике ФГБУ «ВНИИЗЖ», связано с отличающимися параметрами трактовки результатов.
Однако, считаем необходимым обратить внимание, что значение циклов Ct могут изменяться в зависимости от чувствительности набора, целевого детектируемого участка генома вируса АЧС, и чувствительности культуры клеток, на которой проводится определение титра вируса.
Заключение. Как правило, уровень репродукции вируса АЧС определяется титрованием в культуре клеток, поскольку чувствительность РГАд в 10 раз выше (1 ГАдЕ - 10-12 вирионов), чем чувствительность ПЦР-РВ (10 ГАдЕ или ~102вирионов, или ~117 копий), но постановка этой реакции более трудоемка и длительна (7-10 сутки) по сравнению с ПЦР-РВ (2 час 30 минут). Кроме того, несмотря на то, что титрование более чувствительный метод, в определенных случаях, точность результата зависит от чувствительности культуры клеток и квалификации исполнителя.
Выявленная корреляция между значением Ct и титром вируса в пробе позволяет в лабораторной практике использовать ПЦР-РВ для количественного определения содержания вируса в образце, а также, дает возможность детального изучения ряда биологических свойств возбудителя АЧС.
При необходимости использование ПЦР-РВ также дает возможность определить количество копий генома вируса в исследуемых образцах, с поправкой на то, что корреляция должна быть изучена и оптимизирована для определенного набора.
Список литературы:
Резюме. Статья посвящена определению корреляции показателя Ct в ПЦР в режиме реального времени и значений титра вируса, устанавливаемого в реакции гемадсорбции, а также расчету количества копий генома вируса АЧС в образцах. К другим преимуществам ПЦР-РВ относится быстрая и эффективная возможность сравнения и качественной оценки исследуемых образцов. В ряде работ, где показано определение вирулентности вируса по его содержанию в крови, отмечено, что скорость изменения Ct (соответственно, скорость увеличения титра в крови) у аттенуированного вируса ниже, чем у вирулентного. Результаты сравнительного анализа показали высокую стабильность соответствия значений определяемых значений Ct титру вируса и количеству копий генома. По результатам исследований с набором ФБУН «ЦНИИ» изменение концентрации ДНК-копий в 10 раз проводит к изменению значения Ct на 3 цикла. В то же время, снижение титра вируса на 1,0 lg ГАдЕ50/см3 приводит к увеличению показателя Ct в ПЦР в режиме реальном времени на 4 цикла. Для этого с помощью ПЦР был амплифицирован полноразмерный ген B646L вируса АЧС. Выявленная корреляция между значением Ct и титром вируса в пробе позволяет в лабораторной практике использовать ПЦР-РВ для количественного определения содержания вируса в образце, и позволяет детально изучить биологические свойства возбудителя АЧС. Проведено определение соответствия показателей Ct ПЦР-РВ с титром вируса, полученного из крови инфицированного животного вирусом АЧС изолят Krasnodar 07/17. Использование ПЦР-РВ позволяет определять количество копий генома вируса в исследуемых образцах, с поправкой на то, что корреляция должна быть изучена и оптимизирована для определенного набора.
Ключевые слова: вирус африканской чумы свиней, полимеразная цепная реакция в режиме реального времени, реакция гемадсорбции, значения Ct, культура клеток СС, культура клеток КМС, геном вируса АЧС, корреляция, количество копий, биологические свойства, количественный метод.
Сведения об авторах:
Мазлум Али, аспирант референтной лаборатории по АЧС ФГБУ «ВНИИЗЖ»; 600901, г. Владимир, мкр. Юрьевец; e-mail: ali.mazloum6@gmail.com.
Власова Наталья Никифоровна доктор биологических наук, главный научный сотрудник, референтной лаборатории по АЧС ФГБУ «ВНИИЗЖ»; ФГБУ «ВНИИЗЖ»; 600901, г. Владимир, мкр. Юрьевец; e-mail: vlasova_nn@arriah.ru.
Аронова Елена Владимировна, кандидат биологических наук, старший научный сотрудник референтной лаборатории по АЧС ФГБУ «ВНИИЗЖ»; ФГБУ «ВНИИЗЖ»; 600901, г. Владимир, мкр. Юрьевец; e-mail: aronova@arriah.ru.
Иголкин Алексей Сергеевич, кандидат ветеринарных наук, заведующий референтной лабораторией по АЧС ФГБУ «ВНИИЗЖ»; ФГБУ «ВНИИЗЖ»; 600901, г. Владимир, мкр. Юрьевец; e-mail: igolkin_as@arriah.ru. Кривонос Роман Анатольевич, кандидат ветеринарных наук, руководитель департамента ветеринарии Краснодарского края; 350000, г. Краснодар, ул. Рашпилевская, 36; e-mail: sinkubani@mail.ru. Ответственный за переписку с редакцией: Черных Олег Юрьевич, доктор ветеринарных наук, директор ГБУ КК «Кропоткинская краевая ветеринарная лаборатория»; 352380, Краснодарский край, г. Кропоткин, ул. Красноармейская, д. 303; тел.: 8-86138-62314; e-mail: gukkvl50@kubanvet.ru.
|
| 2011 © Ветеринария Кубани | Разработка сайта - Интернет-Имидж | |
|---|---|---|